Raksta medicīnas eksperts
Jaunas publikācijas
Alcheimera slimības cēloņi
Pēdējā pārskatīšana: 06.07.2025

Visi iLive saturs ir medicīniski pārskatīts vai pārbaudīts, lai nodrošinātu pēc iespējas lielāku faktisko precizitāti.
Mums ir stingras iegādes vadlīnijas un tikai saikne ar cienījamiem mediju portāliem, akadēmiskām pētniecības iestādēm un, ja vien iespējams, medicīniski salīdzinošiem pārskatiem. Ņemiet vērā, ka iekavās ([1], [2] uc) esošie numuri ir klikšķi uz šīm studijām.
Ja uzskatāt, ka kāds no mūsu saturiem ir neprecīzs, novecojis vai citādi apšaubāms, lūdzu, atlasiet to un nospiediet Ctrl + Enter.
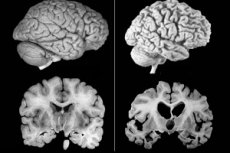
Alcheimera slimība tiek uzskatīta par visizplatītāko ar vecumu saistītās demences veidu: šī patoloģija rodas aptuveni 40% no visām diagnosticētajām demencēm. Pirms simts gadiem šī slimība tika uzskatīta par ļoti retu. Tomēr mūsdienās pacientu skaits strauji pieaug: tik ļoti, ka slimība jau tiek klasificēta kā epidēmiska patoloģija. Un vissliktākais ir tas, ka precīzi Alcheimera slimības cēloņi vēl nav noteikti. Ārsti ceļ trauksmi, jo pietiekamas informācijas trūkums par cēloņiem neļauj apturēt slimības attīstību, kas bieži noved pie pacientu nāves.
Alcheimera slimības cēloņi
Zinātnieki līdz pat šai dienai nav pilnībā noskaidrojuši tādas slimības kā Alcheimera slimības attīstības iemeslus. Ir izvirzīti vairāki pieņēmumi, kas varētu izskaidrot deģeneratīvu reakciju rašanos un tālāku saasināšanos centrālajā nervu sistēmā. Taču neviens no esošajiem pieņēmumiem nav atzīts zinātnieku aprindās.
Diagnozes laikā tiek atklāti smadzeņu darbības traucējumi, kas pavada Alcheimera slimību: tomēr neviens vēl nav spējis noteikt smadzeņu struktūru atrofijas izcelsmes un progresēšanas mehānismus.
Eksperti atzīst, ka Alcheimera slimībai nav viens, bet vismaz vairāki cēloņi. Tās attīstībā galveno lomu spēlē ģenētiski defekti: tas jo īpaši attiecas uz retām slimības formām, kas sāk attīstīties relatīvi agrā vecumā (pirms 65 gadiem).
Iedzimtā Alcheimera slimība tiek pārnesta autosomāli dominējošā veidā. Ar šāda veida pārnešanu slimības parādīšanās varbūtība bērnam ir vienāda ar 50%, retāk – 100%.
Pavisam nesen zinātniekiem izdevās identificēt trīs patogēnus gēnus, kas darbojas kā provokatori agrīnas senilas demences attīstībā. Visbiežāk Alcheimera slimība tiek diagnosticēta, ko izraisa izmaiņas gēnā, kas atrodas XIV hromosomā. Šāds defekts rodas aptuveni 65% pacientu ar šo slimību.
Aptuveni 4% iedzimtas Alcheimera slimības gadījumu ir saistīti ar defektīvu gēnu I hromosomā. Ar šādu defektu slimība ne vienmēr attīstās, bet tikai noteiktu riska faktoru klātbūtnē.
 [ 6 ]
[ 6 ]
Attīstības teorijas
Pēdējo desmitgažu laikā zinātnieki ir veikuši daudz pētījumu par Alcheimera slimības cēloņiem. Tomēr precīzs slimības cēlonis joprojām nav skaidrs. Mūsdienās speciālistiem ir ievērojams teorētisko pieņēmumu saraksts, kas varētu izskaidrot Alcheimera slimības rašanos. Ir skaidri pierādījumi, ka patoloģijai ir heterogēna izcelsme – tas ir, dažiem pacientiem to izraisa iedzimtība, bet citiem – citi iemesli. Ir arī vispārpieņemts, ka slimības agrīna attīstība (pirms 65 gadu vecuma) galvenokārt ir saistīta ar iedzimto tipu. Tomēr šādi iedzimti agrīni varianti ir tikai 10% no kopējā saslimušo skaita.
Ne tik sen zinātnieki veica vēl vienu pētījumu, kura laikā viņiem izdevās identificēt trīs gēnus, kas ir atbildīgi par Alcheimera slimības iedzimto noslieci. Ja cilvēkam ir šī gēnu kombinācija, tad slimības attīstības risks tiek lēsts 100% apmērā.
Bet pat zinātnieku kolosālais sasniegums molekulārās ģenētikas jomā nespēja atbildēt uz jautājumu par Alcheimera slimības attīstību vairumam pacientu.
Kādas teorijas zinātnieki piedāvā, lai atbildētu uz jautājumu par Alcheimera slimības cēloņiem? Ir vairāk nekā ducis šādu teoriju, bet trīs no tām tiek uzskatītas par vadošajām.
Pirmā teorija ir “holīnerģiskā”. Tā ir pamatā lielākajai daļai Alcheimera slimības ārstēšanas metožu. Saskaņā ar šo pieņēmumu slimība attīstās tāda neirotransmitera kā acetilholīna ražošanas samazināšanās dēļ. Nesen šī hipotēze ir saņēmusi lielu skaitu atspēkojumu, un vissvarīgākais no tiem ir tas, ka zāles, kas koriģē acetilholīna trūkumu, nav īpaši efektīvas Alcheimera slimības gadījumā. Domājams, ka organismā notiek arī citi holīnerģiski procesi, piemēram, pilna garuma amiloīdu agregācijas sākšanās un rezultātā ģeneralizēta neiroiekaisšana.
Gandrīz pirms trīsdesmit gadiem zinātnieki ierosināja otru potenciālo teoriju, ko sauca par "amiloida" teoriju. Saskaņā ar šo hipotēzi Alcheimera slimības galvenais cēlonis ir β-amiloida uzkrāšanās. Informācijas nesējs, kas kodē proteīnu, kas kalpo par pamatu β-amiloida veidošanās procesam, ir lokalizēts 21. hromosomā. Kas norāda uz šīs teorijas ticamību? Pirmkārt, fakts, ka visiem indivīdiem ar papildu 21. hromosomu (Dauna sindroms) sasniedzot 40 gadu vecumu, ir patoloģija, kas līdzīga Alcheimera slimībai. Cita starpā APOE4 (slimības pamatfaktors) izraisa pārmērīgu amiloida uzkrāšanos smadzeņu audos, pirms tiek atklātas slimības klīniskās pazīmes. Pat eksperimentu laikā ar transgēniem grauzējiem, kuros tika sintezēts mutēts APP gēna tips, viņu smadzeņu struktūrās tika novērotas fibrilāras amiloida uzkrāšanās. Turklāt grauzējiem tika novēroti arī citi sāpīgi Alcheimera slimībai raksturīgi simptomi.
Zinātniekiem ir izdevies izveidot specifisku serumu, kas attīra smadzeņu struktūras no amiloīdu nogulsnēm. Tomēr tā lietošanai nebija izteiktas ietekmes uz Alcheimera slimības gaitu.
Trešā pamathipotēze bija tau teorija. Ja ticēt šim pieņēmumam, tad virkne Alcheimera slimības traucējumu sākas ar tau proteīna (proteīna tau, MAPT) strukturālu traucējumu. Kā zinātnieki ir norādījuši, maksimāli fosforilētā tau proteīna pavedieni saistās viens ar otru. Tā rezultātā neironos veidojas neirofibrilāri sapīkumi, kas noved pie mikrotubulu integrācijas traucējumiem un intraneironālā transporta mehānisma atteices. Šie procesi izraisa izmaiņas bioķīmiskajā signalizācijā starpšūnu komunikācijā un pēc tam noved pie šūnu nāves.
Alcheimera slimības garīgie cēloņi
Daži eksperti norāda, ka Alcheimera slimība ir amiloīdu olbaltumvielu vielu nogulsnēšanās rezultāts vietās, kur neironi savienojas – sinapsēs. Olbaltumvielas veido noteikta veida savienojumu ar citām vielām, kas, šķiet, savieno neironu iekšpusi un to zarus. Šis process kaitē šūnu normālai darbībai: neirons zaudē spēju uztvert un pārraidīt impulsus.
Saskaņā ar dažu speciālistu, kas nodarbojas ar garīgo praksi, pieņēmumiem, makromolekulu saikne tiek kavēta posmā starp smadzeņu daļu, kas atbild par loģiku, un limfātisko sistēmu. Vienlaikus ar atmiņas, intelekta, orientācijas un runas spējas zudumu cilvēks saglabā sociālo adaptāciju, muzikālo dzirdi un spēju just.
Alcheimera slimība vienmēr parādās dzīves otrajā pusē: tas var nozīmēt, ka tiek zaudēta saikne ar sevi vai arī tā tiek pārnesta uz fizisko līmeni. Pacienti burtiski "iekrīt bērnībā", un tiek atzīmēta acīmredzama degradācija.
Pieaugoši pārtraukumi, kas ietekmē īslaicīgo atmiņu, liecina par atdalīšanos no atbildības par to, kas atrodas tiešajā vidē. Cilvēks, kurš neatceras un dzīvo ārpus realitātes, sākotnēji nevar būt atbildīgs ne par ko. Nesaskaņas iegaumēšanas procesos noved pie tā, ka pacients dzīvo tikai tagadnes brīdī vai arī viņam izdodas savienot pagātni un tagadni. Dzīvošana "šeit un tagad" tipā var kļūt par neatrisināmu problēmu un pat biedējošu. To pašu var teikt par pakāpenisku orientācijas zaudēšanu. Cilvēks saprot, ka vēl nav sasniedzis patieso dzīves mērķi, bet ceļš, pa kuru viņam vajadzētu virzīties, ir zaudēts. Viņš zaudē atskaites punktus savai atrašanās vietai, nezina, kurp ved viņa ceļš. Tā kā ceļotājs neredz gaismu savā ceļā, viņš zaudē arī cerību.
Rezultāts ir atkārtota un ilgstoša depresija un ticības zaudēšana nākotnei.
Tā kā arī paškontrole pakāpeniski izzūd, pacientiem var rasties spontāni emocionāli uzliesmojumi – piemēram, kā mazam bērnam. Visi dzīves laikā attīstītie izglītojošie momenti tiek iznīcināti. Naktī šāds cilvēks var pamosties tumsā, kliedzot, ka nezina savu vārdu un atrašanās vietu.
Runas prasmju zudums var liecināt par nevēlēšanos runāt – galu galā pasaule pacientam neizraisa nekādas citas sajūtas, izņemot apjukumu.
Depresija bieži liecina par relaksāciju, aicinājumu uz pagātni un tagadnes prāta stāvokli. Pacients ar Alcheimera slimību var radīt sev eiforijas sajūtu un ilgstoši tajā palikt.
Tā kā Alcheimera slimība pastiprina ar vecumu saistītās degradācijas parādības, tā parāda sabiedrības vispārējo stāvokli, kas "izdod" arvien vairāk pacientu ar šo slimību. Šāds iespējamais Alcheimera slimības cēlonis kā kalcifikācija var skart gandrīz visus asinsvadus. Olbaltumvielu nogulsnes veidojas daudz agrāk nekā kaļķa, holesterīna vai lipīdu nogulsnes, tāpēc ir jāpievērš visa uzmanība šim faktoram, uzskata daudzi eksperti.
Nāves cēloņi Alcheimera slimības gadījumā
Saskaņā ar jaunāko statistiku, aptuveni 60% Alcheimera slimības pacientu ir predisponēti nāvei trīs gadu laikā pēc slimības sākuma. Mirstības ziņā Alcheimera slimība ieņem 4. vietu pēc sirdslēkmes, insulta un onkoloģijas.
Alcheimera slimība sākas pakāpeniski, gandrīz nemanāmi: paši pacienti atzīmē pastāvīgu noguruma sajūtu un smadzeņu darbības palēnināšanos. Pirmās pazīmes parādās aptuveni 60–65 gadu vecumā, pakāpeniski pieaugot un pasliktinoties.
Nāves cēlonis Alcheimera slimības gadījumā lielākajā daļā gadījumu ir smadzeņu nervu centru, kas ir atbildīgi par dzīvībai svarīgu orgānu darbību, mazspēja. Piemēram, pacientam var attīstīties smagi gremošanas sistēmas darbības traucējumi, zust tā sauktā muskuļu atmiņa, kas ir atbildīga par sirdsdarbību un plaušu darbību. Rezultātā var rasties sirdsdarbības apstāšanās, sastrēguma pneimonija vai citas dzīvībai bīstamas komplikācijas.
Alcheimera slimības patoģenēze
Kā jau iepriekš minējām, zinātniekiem nav precīzu, pārbaudītu datu par patiesajiem Alcheimera slimības cēloņiem. Tomēr fakts, ka slimības straujā attīstība notiek vecumdienās, jau var tikt uzskatīts par zināmu atkarību no vecuma. Ar vecumu saistītas izmaiņas var uzskatīt par galveno Alcheimera slimības riska faktoru.
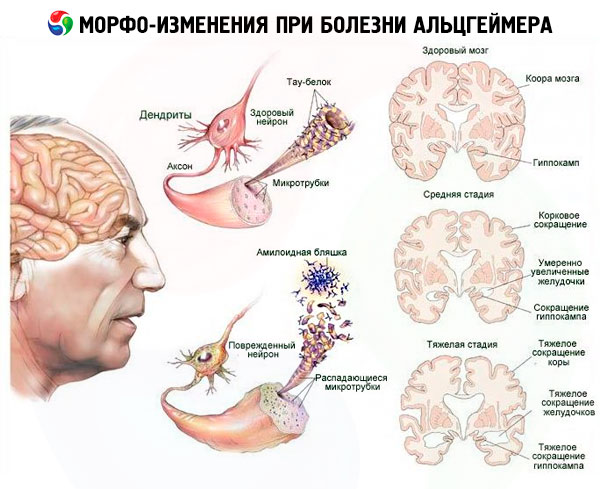
Šādus faktorus var uzskatīt par pilnīgi neatgriezeniskiem:
- vecums (saskaņā ar statistiku, cilvēkiem, kas vecāki par 90 gadiem, Alcheimera slimība tiek atklāta vairāk nekā 40% gadījumu);
- pieder pie sieviešu dzimuma;
- iepriekšējas traumatiskas smadzeņu traumas, tostarp galvaskausa bojājumi dzemdību laikā;
- smags stress;
- bieža vai ilgstoša depresija;
- vāja intelektuālā attīstība (piemēram, izglītības trūkums );
- zema garīgā aktivitāte visas dzīves laikā.
Teorētiski koriģējami faktori ir šādi:
- pārmērīgs spiediens uz asinsvadiem hipertensijas un/vai aterosklerozes dēļ;
- hiperlipidēmija;
- augsts cukura līmenis asinīs, diabēts;
- elpošanas vai koronāro artēriju slimības, kas veicina ilgstošas hipoksijas stāvokli.
Cilvēks var samazināt Alcheimera slimības attīstības risku, ja viņš vai viņa novērš visbiežāk sastopamos riska faktorus:
- liekais svars;
- fiziskās aktivitātes trūkums;
- pārmērīga kofeīna uzņemšana;
- smēķēšana;
- zema garīgā aktivitāte.
Diemžēl ir pierādīts fakts: nezināšana un šaurs skatījums var tieši ietekmēt slimības attīstību. Zems intelekts, slikta runas spēja, šaurs skatījums – arī šie ir iespējamie Alcheimera slimības cēloņi.
Alcheimera slimības patogēnās īpašības
- Alcheimera slimības neiropatoloģiskās iezīmes.
Sākoties slimībai, tiek novērota nervu šūnu zudums, tiek traucēti sinaptiskie savienojumi pusložu garozā un atsevišķās subkortikālās zonās. Kad neironi iet bojā, bojātās zonas atrofējas, tiek novēroti deģeneratīvi procesi, kas ietekmē temporālās un parietālās daivas, cingulārās garozas frontālās daļas laukumu un cingulāro vijumu.
Amiloīda nogulsnes un neirofibrilārus samezglojumus var redzēt mikroskopā pēcnāves izmeklēšanas laikā. Nogulsnes izskatās kā amiloīda un šūnu elementu kondensācijas neironu iekšpusē un uz to virsmas. Šūnās tās palielinās, veidojot šķiedrainas, blīvas struktūras, ko dažreiz sauc par samezglojumiem. Gados vecākiem cilvēkiem šie nogulumi bieži ir smadzenēs, bet pacientiem ar Alcheimera slimību to ir īpaši daudz, bieži vien noteiktās smadzeņu zonās (piemēram, temporālajās daivās).
- Alcheimera slimības bioķīmiskās īpašības.
Zinātnieki ir noskaidrojuši, ka Alcheimera slimība ir proteinopātija – patoloģija, kas saistīta ar patoloģiski strukturētu olbaltumvielu, tostarp β-amiloida un tau proteīna, uzkrāšanos smadzeņu struktūrās. Uzkrājumus veido mazi peptīdi, kuru garums ir 39–43 aminoskābes: tos sauc par β-amiloidiem. Tie ir prekursora proteīna APP daļas – transmembrānas proteīna, kas iesaistīts nervu šūnu attīstībā un reģenerācijā. Pacientiem ar Alcheimera slimību APP tiek pakļauts proteolīzei, izmantojot joprojām neskaidrus mehānismus, daloties peptīdos. Peptīda veidotās β-amiloida šķiedras salīp kopā starp šūnām, veidojot sablīvējumus – tā sauktās senilās plāksnes.
Saskaņā ar citu klasifikāciju, Alcheimera slimība arī pieder pie tauopātiju klases – slimībām, kas saistītas ar nepareizu, patoloģisku tau proteīna agregāciju. Katrai nervu šūnai ir šūnu skelets, kas daļēji sastāv no mikrocaurulītēm. Šīs caurulītes darbojas kā sava veida vadotne barības vielām un citām vielām: tās savieno šūnas centru ar tās perifēriju. Tau proteīns kopā ar dažiem citiem proteīniem uztur saikni ar mikrocaurulītēm – piemēram, tas ir to stabilizators pēc fosforilēšanas reakcijas. Alcheimera slimībai raksturīga pārmērīga, maksimāla fosforilēšanās, kas noved pie olbaltumvielu pavedienu salipšanas. Savukārt tas izjauc transporta mehānismu nervu šūnā.
- Alcheimera slimības patoloģiskās īpašības.
Nav datu par to, kā amiloīdu peptīdu ražošanas traucējumu un turpmākas uzkrāšanās mehānisms noved pie Alcheimera slimībai raksturīgām patoloģiskām izmaiņām. Amiloīdu uzkrāšanās tika pozicionēta kā galvenā saikne nervu šūnu deģeneratīvajā procesā. Iespējams, uzkrāšanās traucē kalcija jonu homeostāzi, kas noved pie apoptozes. Vienlaikus tika atklāts, ka amiloīds uzkrājas mitohondrijos, bloķējot atsevišķu enzīmu darbību.
Iekaisuma reakcijām un citokīniem, iespējams, ir ievērojama patofizioloģiska nozīme. Iekaisuma procesu pavada neizbēgami audu bojājumi, taču Alcheimera slimības gaitā tam ir sekundāra loma vai tas ir imūnās atbildes indikators.
- Alcheimera slimības ģenētiskās īpašības.
Ir identificēti trīs gēni, kas ir atbildīgi par Alcheimera slimības agrīnu attīstību (pirms 65 gadu vecuma). Galvenā loma tiek piešķirta APOE, lai gan ne visi slimības gadījumi ir saistīti ar šo gēnu.
Mazāk nekā 10% agrīnā stadijā esošo slimību ir saistītas ar ģimenes mutācijām. Izmaiņas ir konstatētas gēnos APP, PSEN1 un PSEN2, kas galvenokārt paātrina neliela proteīna, ko sauc par abeta42, izdalīšanos, kas ir galvenā amiloīdu nogulšņu sastāvdaļa.
Atklātie gēni neliecina par predispozīciju, bet daļēji palielina risku. Visizplatītākais ģenētiskais faktors tiek uzskatīts par ģimenes alēli E4, kas saistīta ar APOE gēnu. Gandrīz 50% slimības attīstības gadījumu ir saistīti ar to.
Zinātnieki vienbalsīgi uzskata, ka citi gēni ar dažādu varbūtības pakāpi ir saistīti ar Alcheimera slimības attīstību. Šobrīd speciālisti ir analizējuši aptuveni četrsimt gēnu. Piemēram, viena no atklātajām RELN variācijām ir iesaistīta Alcheimera slimības attīstībā sievietēm pacientēm.

