Raksta medicīnas eksperts
Jaunas publikācijas
Kateholamīnu sintēze, sekrēcija un metabolisms
Pēdējā pārskatīšana: 19.10.2021

Visi iLive saturs ir medicīniski pārskatīts vai pārbaudīts, lai nodrošinātu pēc iespējas lielāku faktisko precizitāti.
Mums ir stingras iegādes vadlīnijas un tikai saikne ar cienījamiem mediju portāliem, akadēmiskām pētniecības iestādēm un, ja vien iespējams, medicīniski salīdzinošiem pārskatiem. Ņemiet vērā, ka iekavās ([1], [2] uc) esošie numuri ir klikšķi uz šīm studijām.
Ja uzskatāt, ka kāds no mūsu saturiem ir neprecīzs, novecojis vai citādi apšaubāms, lūdzu, atlasiet to un nospiediet Ctrl + Enter.
Nervu smadzeņu slānis rada savienojumu tālu no struktūras steroīdiem. Tie satur 3,4-dihidroksifenilu (katehola) kodolu un sauc par kateholamīniem. Tie ietver adrenalīnu, norepinefrīnu un dopamīnu beta-okstiramīnu.
Sequence kateholamīns sintēze ir diezgan vienkāršs: tirozīns → dihydroxyphenylalanine (DOPA) → → dopamīna norepinefrīna → adrenalīna. Tirozīns iekļūst ķermenī ar uzturu, bet to var arī veidot no fenilalanīna aknās zem fenilalanīna hidroksilāzes darbības. Galīgie tirozīna transformācijas produkti audos ir atšķirīgi. In virsnieru serdē process pāriet pie soļa adrenalīna veidošanos, galos simpātiskās nervu - noradrenalīna, dažos neironos centrālās nervu sistēmas kateholamīnu dopamīna sintēzes aizpildītu veidlapu.
Tirozīna pārvēršana DOPA katalizē tirozīna hidroksilāze, kuras kofaktori ir tetrahidro-biopterīns un skābeklis. Tiek uzskatīts, ka tieši šis enzīms ierobežo visa kateholamīna biosintēzes procesa ātrumu un tiek kavēts procesa gala produktos. Tirozīna hidroksilāze ir galvenais regulējošo iedarbību uz kateholamīnu biosintēzi.
Dopa uz dopamīna konversijas katalizē ar enzīmu dopa dekarboksilāzes (kofaktors - piridoksāls), kas ir samērā nespecifiskas un decarboxylated, un cits aromātisks L-amino acid. Tomēr ir norādes par iespēju mainīt kateholamīnu sintēzi, mainot aktivitāti un šo enzīmu. Dažos neironos nav dermatīta pārveidošanas enzīmu, un tas ir gala produkts. Citi audu sastāvā ir dopamīns-beta-hidroksilāze (kofaktors - varš, askorbīnskābe un skābeklis), kas pārveido dopamīnu par norepinefrīnu. Nepilngadīgo medulla (bet ne simpātisko nervu galā) ir feniletanolamīns - metiltransferāze, kas rada nerezidējošu adrenalīnu. Metilgrupu donors šajā gadījumā ir S-adenosilmetionīns.
Ir svarīgi atcerēties, ka sintēze phenylethanolamine-N-Metiltransferazy inducē glikokortikoīdus, kas ietilpst smadzeņu garozas slānī portāla venozās sistēmas. Tas var izskaidrot faktu melus apvieno divus dažādus endokrīno dziedzeru vienā organismā. Nozīme glikokortikoīdu sintēzes adrenalīna uzsver fakts, ka virsnieru serde šūnas, kas ražo norepinefrīna izkārtoti ap arteriālo kuģiem, kamēr asins šūnas ir iegūtas adrenalinprodutsiruyuschie būtībā venozās dobumu, lokalizētas virsnieru garozas.
Par kateholamīnu sabrukums notiek galvenokārt reibumā divu enzīmu sistēmām: katehol-O-metiltransferāze (KOMT) un monoamīnoksidāzes (MAO). Galvenie veidi epinefrīna un norepinefrīna pūšanas shematiski parādīts attēlā. 54. Saskaņā ar darbības KOMT klātbūtnē donora metilgrupām S-adrenozilmetionina kateholamīnu un pārvērš normetanephrine metanephrine (3-O-metil-atvasinājumiem epinefrīna un norepinefrīna), kas reibumā MAO pārveidots aldehīdu un vairāk (klātbūtnē aldehīdu) in vanillyl-mandeļskābe acid (ICH) - galvenais noārdīšanās produkts, noradrenalīna un adrenalīna. Šajā pašā lietā, kad pirmo reizi saskaras ar kateholamīnu MAO darbības, nevis COMT, tie tiek konvertēti uz 3,4-dioksimindalevy aldehīds, un pēc tam reibumā aldehīdu un KOMT - 3,4-dioksimindalnuyu skābi un IUS. In klātbūtnē alkohola dehidrogenāzes kateholamīnu var veidot 3-metoksi-4-oksifenilglikol, galvenais galaprodukts degradāciju epinefrīna un norepinefrīna CNS.
Dezintegrācijas dopamīna norit līdzīgi, izņemot to, ka tā metabolīti ir nepiemīt hidroksilgrupām uz beta-oglekļa atomu, un tādēļ, tā vietā, lai vanillyl-mandeļskābe veidojas homovanillic (HVA) un 3-metoksi-4-oksifeniluksusnaya skābi.
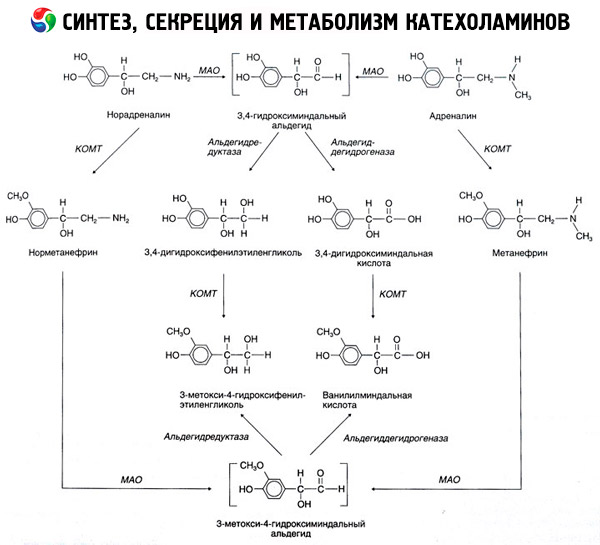
Var pierādīt arī, ka pastāv kvinoids ceļš kateholamīnu molekulas oksidēšanai, kurā var būt arī starpprodukti ar izteiktu bioloģisko aktivitāti.
Veido rīcībai citosolisko enzīmu, adrenalīna un noradrenalīna simpātisks nervu galiem, virsnieru serdes un ievadiet sekretorajām granulas, kas aizsargā tos no darbības sadalīšanās fermentiem. Kateholamīnu sagūstīšana ar granulām prasa enerģijas izmaksas. In hromafīnās granulām virsnieru iegarenās kateholamīnu cieši saistās ar ATP (proporcijā 4: 1) un specifisku proteīnu - chromogranin kas novērš difūziju hormonu no granulām citoplazmā.
Direct stimulēšanas uz sekrēcijas kateholamīnu acīmredzot iespiešanās kalcija šūnu stimulējot eksocitozes ceļā (saplūšana membrānu granulas ar šūnu virsmas un to atšķirību ar kopējo ražu šķīstoša saturu - kateholamīnu, dopamīna-beta-hidroksilāzes, ATP un Chromogranin - uz ārpusšūnu šķidrumā) .
Kateholamīnu fizioloģiskais efekts un to iedarbības mehānisms
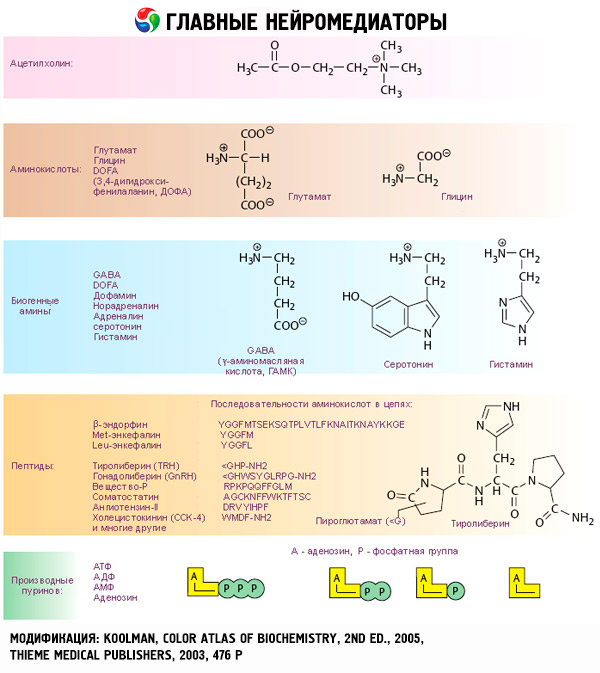
Kateholamīnu iedarbība sākas ar mijiedarbību ar specifiskiem mērķa šūnu receptoriem. Ja vairogdziedzera un steroīdu hormonu receptori tiek lokalizēti šūnu iekšienē, ārējā šūnu virsmā atrodas kateholamīnu receptori (kā arī acetilholīns un peptīdu hormoni).
Tas jau sen ir pierādīts, ka attiecībā uz kādu reakciju adrenalīnu vai noradrenalīnu ir efektīvāki nekā sintētisko kateholamīnu izoproterenolu, bet citiem efekts ir pārāka par darbības izoproterenolu epinefrīna vai norepinefrīnu. Pamatojoties uz šo koncepciju, lai klātbūtni divu veidu audos ir izstrādāta adrenerģiskās alfa un beta, un tikai kāds no šiem diviem veidiem var būt klāt dažās no tām. Izoproterenolu ir visvairāk spēcīgs agonists no beta-adrenoreceptoru, tā sintētisku savienojumu fenilefrīnu - visspēcīgāko agonists no alfa-adrenoreceptoru. Dabas kateholamīnu - adrenalīna un noradrenalīna - spēj mijiedarboties ar receptoriem abiem veidiem, bet adrenalīns notiek lielāka afinitāte pret beta, un norepinefrīna - alfa receptori.
Kateholamīnu spēcīgāki aktivizēt sirds beta-adrenerģiskos receptorus nekā beta receptoriem gludo muskulatūru, ļaujot beta-tipa sadalīts apakštipi: bēta1 receptori (sirds, tauku šūnas) un bēta2 receptoriem (bronhu, asinsvadiem, utt ...). Par izoproterenolu par Beta1 receptoru augstākās rīcību adrenalīna un noradrenalīna tikai 10 reizes rīcību, kamēr bēta2 receptoriem tas darbojas 100-1000 reižu iedarbīgāks nekā dabiskā kateholamīnu.
Konkrētu antagonistu (fentolamīns un fenoksibenzamīns pret alfa un propranololu beta receptoriem) izmantošana apstiprināja adrenoreceptoru klasifikācijas atbilstību. Dopamīns ir spējīgs mijiedarboties gan ar alfa un beta receptoriem, bet dažādos audos (smadzenēs, hipofīzes, kuģi) atrastas un pašu dopamīnerģiskiem receptoriem īpašu bloķētājs, kas ir haloperidols. Beta receptoru skaits ir no 1000 līdz 2000 uz vienu šūnu. Beta receptoru izraisīto kateholamīnu bioloģiskie efekti parasti ir saistīti ar adenilāta ciklāzes aktivizēšanu un cAMP intracelulārā satura palielināšanos. Receptors un enzīms, lai arī tie ir funkcionāli saistīti, bet pārstāv dažādas makromolekulas. Adenilāta ciklazas aktivitātes modulācijā hormona-receptora kompleksa ietekmē tiek iesaistīti guanosīna trifosfāti (GTP) un citi purīna nukleotīdi. Palielinot fermenta aktivitāti, šķiet, ka tie samazina agonistu beta receptoru afinitāti.
Jau zināms, ka denervētu struktūru jutīguma palielināšanas fenomens ir zināms. Savukārt ilgstoša agonistu iedarbība samazina mērķa audu jutīgumu. Pētījums par beta receptoriem ļāva izskaidrot šīs parādības. Tika parādīts, ka ilgstoša izoproterenola darbība izraisa adenilāta ciklāzes jutības zudumu, jo ir samazinājies beta receptoru skaits.
Desensibilizācijas procesam nav nepieciešams aktivēt proteīnu sintēzi un, iespējams, ir saistīts ar pakāpenisku neatgriezenisku hormonu receptoru kompleksu veidošanos. Gluži pretēji, 6-oksidofamīna, kas sadala simpātiskos galus, ievadīšanu papildina reaģējošo beta receptoru skaita palielināšanās audos. Nav izslēgts, ka simpatītu nervu aktivitātes palielināšanās nosaka ar vecumu saistīto asinsvadu un tauku audu desensitizāciju attiecībā pret kateholamīniem.
Adrenoreceptoru skaitu dažādos orgānos var kontrolēt ar citiem hormoniem. Tātad, tas palielina estradiola, progesterona un samazināt skaitu alfa adrenoreceptoru dzemdē, kas ir kopā ar atbilstošu palielinājumu vai samazinājumu, tās saraušanās atbildot uz kateholamīnu. Ja intracelulārais "otrais kurjers", kas veidojas ar β receptoru agonistu iedarbību, noteikti ir cAMP, tad sarežģītāks ir alfa-adrenerģiskās ietekmes raidītāja gadījums. Tiek pieņemts, ka pastāv dažādi mehānismi: cAMP līmeņa pazemināšanās, cAMP satura palielināšanās, kalcija šūnu dinamikas modulācija,
Lai reproducētu dažādus ķermeņa efektus, parasti jālieto adrenalīna devas, kas ir 5-10 reizes zemākas nekā norepinefrīns. Lai gan tā ir daudz efektīvāka attiecībā uz A un bēta1 adrenoreceptoru, ir svarīgi atcerēties, ka gan endogēnās kateholamīns spēj mijiedarboties gan ar alfa un beta-receptoru. Tādēļ šī ķermeņa bioloģiskā reakcija pret adrenerģisko aktivāciju lielā mērā ir atkarīga no tajā esošo receptoru tipa. Tomēr tas nenozīmē, ka simpātiskās-virsnieru sistēmas nervu vai humorālās saites selektīva aktivizēšana nav iespējama. Vairumā gadījumu tā dažādo saišu aktivitāte ir intensīvāka. Tādējādi, tiek pieņemts, ka tas aktivizē refleksa hipoglikēmija virsnieru serdē, tā kā asinsspiediena pazemināšanās (ortostatiska hipotensija) pievieno galvenokārt norepinefrīna atbrīvošanu no simpātiskās nervu galiem.
Adrenoreceptori un to aktivācijas efekti dažādos audos
|
Sistēma, orgāns |
Adrenoreceptoru tips |
Reakcija |
|
Sirds un asinsvadu sistēma: |
||
|
Sirds |
Beta |
Kontrakciju biežuma, vadīšanas un kontraktilitātes palielināšanās |
|
Arterioli: |
||
|
āda un gļotādas |
Alfa |
Samazinājums |
|
No skeleta muskuļiem |
Beta |
Paplašināšanas samazināšana |
|
Vēdera orgāni |
Alfa (vairāk) |
Samazinājums |
|
Beta |
Pagarinājums |
|
|
Vēnas |
Alfa |
Samazinājums |
|
Elpošanas sistēma: |
||
|
Bronhu muskuļi |
Beta |
Pagarinājums |
|
Gremošanas sistēma: |
||
|
Kuņģis |
Beta |
Samazināta motora funkcija |
|
Zarnas |
Alfa |
Sfinkteru samazināšana |
|
Spleenis |
Alfa |
Samazinājums |
|
Beta |
Relaksācija |
|
|
Ārēji aizkuņģa dziedzera daļa |
Alfa |
Samazināts sekrēts |
|
Dzemdes kakla sistēma: |
Alfa |
Sfinktera samazināšana |
|
Urīnpūšļa |
Beta |
Relaksējoša eksorcista muskuļa |
|
Vīriešu dzimumorgāni |
Alfa |
Ejakulācija |
|
Acis |
Alfa |
Skolēns paplašināts |
|
Āda |
Alfa |
Paaugstināta svīšana |
|
Zarnu dziedzeri |
Alfa |
Kālija un ūdens izdalīšana |
|
Beta |
Amilāzes sekrēcija |
|
|
Endokrīni dziedzeri: |
||
|
Aizkuņģa dziedzera saliņas |
||
|
Beta šūnas |
Alfa (vairāk) |
Samazināts insulīna sekrēcija |
|
Beta |
Paaugstināta insulīna sekrēcija |
|
|
Alfa šūnas |
Beta |
Paaugstināta glikagona sekrēcija |
|
8-šūnas |
Beta |
Paaugstināta somatostatīna sekrēcija |
|
Hipotalāmu un hipofīzes: |
||
|
Somatotrofi |
Alfa |
STH sekrēcijas palielināšanās |
|
Beta |
Samazināts STH sekrēcija |
|
|
Laktotrofi |
Alfa |
Samazināta prolaktīna sekrēcija |
|
Tirotrofi |
Alfa |
Samazināts TSH sekrēcija |
|
Kortikotrofi |
Alfa |
Paaugstināta AKTH sekrēcija |
| beta | Samazināts ACTH sekrēcija | |
|
Vairogdziedzera darbība: |
||
|
Folikulu šūnas |
Alfa |
Samazināta tiroksīna sekrēcija |
|
Beta |
Paaugstināta tiroksīna sekrēcija |
|
|
Parafolikulāri (K) šūnas |
Beta |
Palielināta kalcitonīna sekrēcija |
|
Paratheedēmas dziedzeri |
Beta |
Paaugstināta PTH sekrēcija |
|
Nieres |
Beta |
Palielināta renīna sekrēcija |
|
Kuņģis |
Beta |
Palieliniet gastrīna sekrēciju |
|
Pamata apmaiņa |
Beta |
Skābekļa patēriņa pieaugums |
|
Aknas |
? |
Glikogenolīzes un glikoneoģenēzes pieaugums no glikozes produkcijas; palielina ketogēni, atbrīvojot ketonu ķermeņus |
|
Adipoza audi |
Beta |
Lipolīzes pieaugums, atbrīvojot brīvās taukskābes un glicerīnu |
|
Skeleta muskuļi |
Beta |
Glikolīzes līmeņa paaugstināšanās ar piruvāta un laktāta izdalīšanos; proteolīzes pazemināšanās ar alanīna, glutamīna iznākuma samazināšanos |
Ir svarīgi paturēt prātā, ka intravenozas kateholamīnu rezultāti ne vienmēr ir adekvāti atspoguļotu ietekmi endogēno savienojumu. Tas attiecas galvenokārt uz noradrenalīna, jo tas stāv organismā lielākoties nav asinīs, bet tieši sinaptisko plaisa. Tāpēc endogēnas norepinefrīna aktivizē, piemēram, ne tikai asinsvadu alfa receptorus (paaugstināts asinsspiediens), bet arī sirds beta-receptoru (paātrināta sirdsdarbība), turpretī ievadīšanas noradrenalīna spailēm galvenokārt aktivāciju asinsvadu alfa receptoru un refleksu (caur Vagus) palēnināta sirdsklauves.
Zemas epinefrīna devas galvenokārt aktivizē muskuļu trauku un sirds beta receptorus, kā rezultātā samazinās perifēro asinsvadu pretestība un palielinās sirds minūtes tilpums. Dažos gadījumos pirmais efekts var dominēt, un pēc adrenalīna ievadīšanas attīstās hipotensija. Augstās devās adrenalīns aktivē arī alfa receptorus, ko papildina perifēro asinsvadu rezistences palielināšanās, un sirds minūtes skaita palielināšanās fons palielina asinsspiedienu. Tomēr saglabājas arī tā ietekme uz asinsvadu beta receptoriem. Tā rezultātā sistoliskā spiediena palielināšanās pārsniedz diastolisko spiedienu (impulsa spiediena palielināšanās). Ar pat lielāku devu ieviešanu sāk dominēt epinefrīna alfa-mimetiskie efekti: sistoliskais un diastoliskais spiediens palielinās paralēli gan noradrenalīna ietekmē.
Kateholamīnu ietekme uz vielmaiņu tiek veidota no to tiešas un netiešas ietekmes. Pirmie tiek realizēti galvenokārt ar beta receptoriem. Sarežģītāki procesi ir saistīti ar aknām. Kaut arī aknu glikogenolīzes uzlabošana tradicionāli tiek uzskatīta par beta-receptora aktivācijas rezultātu, tajā ir arī dati par alfa receptoru iesaistīšanos. Kateholamīnu mediētais efekts ir saistīts ar daudzu citu hormonu, piemēram, insulīna, sekrēcijas modulāciju. Adrenalīna darbība pēc tās sekrēcijas acīmredzami pārsvarā ir alfa-adrenerģiskā sastāvdaļa, jo ir pierādīts, ka jebkura stresa dēļ tiek kavēta insulīna sekrēcija.
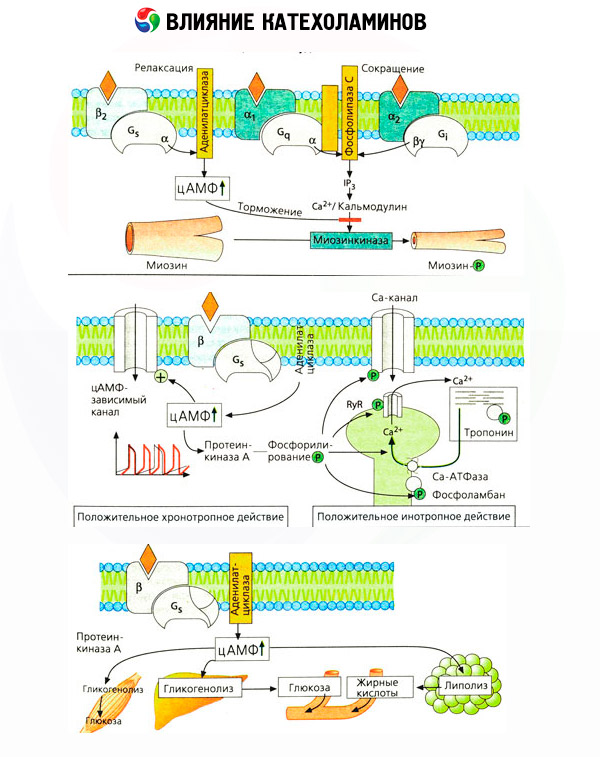
Kateholamīnu tiešās un mediētās iedarbības kombinācija izraisa hiperglikēmiju, kas saistīta ne tikai ar glikozes līmeņa paaugstināšanos aknās, bet arī ar perifēro audu lietošanas kavēšanu. Lipolīzes paātrināšana izraisa hiperlipidēmiju, palielinot taukskābju piegādi aknām un pastiprinot ketonu ķermeņu ražošanu. Stiprināšana glikolīzi muskuļos izraisa palielinātu produkcijas asins laktāta un piruvātā, kas kopā ar glicerīnu, kas izdalās no taukaudiem, ir priekšgājēji aknu glikoneoģenēzes.
Kateholamīnu sekrēcijas regulēšana. To izstrādājumu un metodēm, reaģējot uz simpātiskās nervu sistēmas un virsnieru serdē līdzība bija pamats apvienojot šīs struktūras vienā ķermeņa sympathoadrenal sistēma atbrīvošanas nervu un hormonu tās saiti. Various centrtieces signāli tiek koncentrēta hipotalāma un centriem muguras smadzeņu un iegarenās smadzenes no un kas iegūti eferento paku pārslēgšanos uz preganglionic neirons šūnu organizācijām, kas atrodas sānu raga muguras smadzeņu līmenī kakla VIII - II-III jostas segmentos.
Preganglionic axons no šīm šūnām, kas atstāj muguras smadzeņu un veido sinaptiskā savienojumus ar neironi ir lokalizētas saknīti simpātiskās ķēdi, vai virsnieru iegarenās šūnām. Tie ir cholinergic preganglionic šķiedras. Pirmais būtiska atšķirība postgangliju simpātisks neironu un virsnieru serdes hromafīnās šūnas sastāv ka tā tiek nosūtīta uz ienākošo signālu tas holīnerģisku neiro-vadāmības (postgangliju adrenerģiskajai nervu), un šķidrumu, iezīmējot adrenerģiskās savienojums ar asinīm. Otra atšķirība ir samazināts līdz postgangliju nervu, kas ražo norepinefrīna, kamēr virsnieru serde šūnām - vēlams adrenalīnu. Šīs divas vielas atšķirīgi ietekmē audumu.

