Jaunas publikācijas
Jauni pierādījumi veicina izpratni par Reta sindroma cēloņiem
Pēdējā pārskatīšana: 14.06.2024

Visi iLive saturs ir medicīniski pārskatīts vai pārbaudīts, lai nodrošinātu pēc iespējas lielāku faktisko precizitāti.
Mums ir stingras iegādes vadlīnijas un tikai saikne ar cienījamiem mediju portāliem, akadēmiskām pētniecības iestādēm un, ja vien iespējams, medicīniski salīdzinošiem pārskatiem. Ņemiet vērā, ka iekavās ([1], [2] uc) esošie numuri ir klikšķi uz šīm studijām.
Ja uzskatāt, ka kāds no mūsu saturiem ir neprecīzs, novecojis vai citādi apšaubāms, lūdzu, atlasiet to un nospiediet Ctrl + Enter.

Reta sindroms ir reti sastopams neiroloģiskās attīstības traucējums, kuru pašlaik nevar izārstēt vai labi ārstēt. Tas izraisa smagus fiziskus un kognitīvus simptomus, no kuriem daudzi pārklājas ar autisma spektra traucējumiem.
Reta sindromu izraisa mutācijas MECP2 gēnā, kas ir ļoti izteikts smadzenēs un, šķiet, spēlē svarīgu lomu neironu veselības uzturēšanā. Gēns atrodas X hromosomā, un sindroms galvenokārt skar meitenes. Lai izstrādātu Reta sindroma ārstēšanu, pētnieki vēlas labāk izprast MECP2 un tā funkcijas smadzenēs.
Pētnieki, tostarp Vaithedas institūta līdzdibinātājs Rūdolfs Jaenišs, ir pētījuši MECP2 gadu desmitiem, tomēr daudzi pamata fakti par gēnu palika nezināmi. MECP2 proteīns, ko kodē gēns, ir iesaistīts gēnu regulēšanā; tas saistās ar DNS un ietekmē dažādu citu gēnu ekspresijas līmeņus, proti, to ražoto olbaltumvielu daudzumu.
Tomēr pētniekiem nebija pilnīga saraksta ar gēniem, kurus ietekmē MECP2, un nebija vienprātības par to, kā MECP2 ietekmē šos gēnus.
Agrīnie MECP2 pētījumi liecināja, ka tas ir represors, kas samazina tā mērķa gēnu ekspresiju, bet Jaenisch un citu pētījumi iepriekš bija parādījuši, ka MECP2 darbojas arī kā aktivators, palielinot tā mērķu ekspresiju, un ka tas var vispirms esi aktivators. Tāpat nebija zināms MECP2 darbības mehānisms vai tas, ko tieši dara proteīns, kas izraisa izmaiņas gēnu ekspresijā.
Tehnoloģiju ierobežojumi nav ļāvuši pētniekiem iegūt skaidrību par šiem jautājumiem. Taču Janišs, pēcdoktors savā laboratorijā Yi Liu un bijušais Jaņiša laboratorijas loceklis Entonijs Flamjē, tagad Monreālas Universitātes CHU Sainte-Justine pētniecības centra docents, ir izmantojuši vismodernākās metodes, lai atbildētu uz šiem jautājumiem. Atlikušie jautājumi par MECP2 un gūt jaunus ieskatus par tā lomu smadzeņu veselībā un slimībās.
To rezultāti tika publicēti žurnālā Neuron, un pētnieki arī izveidoja savu MECP2 datu tiešsaistes krātuvi — portāls MECP2-NeuroAtlas kā resurss citiem pētniekiem.
"Es domāju, ka šis dokuments būtiski mainīs to, kā cilvēki domā par to, kā MECP2 izraisa Reta sindromu. Mums ir pilnīgi jauna izpratne par mehānismu, un tas var sniegt jaunas iespējas šīs slimības ārstēšanas izstrādē," saka Jaenisch, kurš ir arī bioloģijas profesors Masačūsetsas Tehnoloģiju institūtā.
Padziļināta izpratne par MECP2 smadzenēs
Pētnieki vispirms izveidoja detalizētu karti, kur MECP2 saistās cilvēka neironu gēnu secībā vai nu gēnos, vai to tuvumā esošajos DNS regulējošajos reģionos. Viņi izmantoja pieeju, ko sauc par CUT&Tag, kas var noteikt proteīna un DNS mijiedarbību ar augstu precizitāti.
Pētnieki ir atklājuši vairāk nekā četrus tūkstošus gēnu, kas saistīti ar MECP2. Viņi atkārtoja savu kartēšanu neironos ar parastajām MECP2 mutācijām, kas saistītas ar Reta sindromu, lai noteiktu, kur slimības stāvoklī MECP2 ir izsmelts.
Zinot, ar kuriem gēniem MECP2 saistās, Liu un Flamier varēja sākt veidot savienojumus starp MECP2 mērķiem un smadzeņu veselību. Viņi atklāja, ka daudzi tā mērķi ir iesaistīti neironu aksonu un sinapsu attīstībā un darbībā.
Viņi arī salīdzināja savu MECP2 mērķu sarakstu ar Simons Foundation Autism Research Initiative (SFARI) ar autismu saistīto gēnu datubāzi un atklāja, ka 381 gēns šajā datubāzē ir MECP2 mērķi.
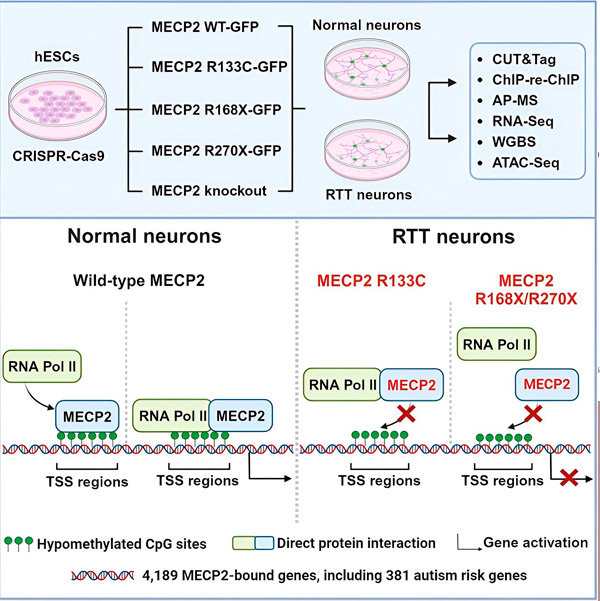
Avots: Neuron (2024). DOI: 10.1016/j.neuron.2024.04.007
Šie atklājumi var palīdzēt noskaidrot Reta sindroma autisma simptomu pamatā esošos mehānismus un nodrošināt labu sākumpunktu MECP2 iespējamās lomas izpētei autismā.
"Mēs esam izveidojuši pirmo integrēto MECP2 epigenoma karti veselības un slimību jomā, un šī karte var vadīt turpmākos pētījumus," saka Liu. "Zinot, kuri gēni ir vērsti uz MECP2 un kuri gēni ir tieši traucēti slimības laikā, nodrošina spēcīgu pamatu Reta sindroma izpratnei un jautājumu uzdošanai par gēnu regulēšanu neironos."
Pētnieki arī pārbaudīja, vai MECP2 palielina vai samazina mērķa gēnu ekspresiju. Atbilstoši tam, ka daži MECP2 ir identificējuši kā aktivatoru, bet citi kā represoru, Liu un Flamjē atrada piemērus, kur MECP2 spēlē abas lomas.
Tomēr, lai gan MECP2 biežāk tiek uzskatīts par represoru, Liu un Flamjē atklāja, ka tas galvenokārt ir aktivators — apstiprinot Jaeniša un Liu iepriekšējos atklājumus. Viens jauns eksperiments parādīja, ka MECP2 aktivizē vismaz 80% no saviem mērķiem, bet otrs, ka tas aktivizē līdz 88% no saviem mērķiem.
Pētnieku izveidotā mērķa gēnu karte sniedza papildu ieskatu MECP2 kā aktivatora lomā. Viņi atklāja, ka gēniem, kurus MECP2 aktivizē, tas parasti saistās ar DNS reģionu augšpus gēna, ko sauc par transkripcijas sākuma vietu.
Šajā vietā šūnu mašīnas uzsāk gēna nolasīšanas procesu RNS, pēc tam RNS tiek pārvērsta funkcionālā proteīnā, kas ir gēnu ekspresijas produkts. MECP2 klātbūtne transkripcijas sākuma vietā, kur sākas gēnu ekspresija, atbilst tā kā gēnu aktivatora lomai.
Pētnieki nolēma noteikt MECP2 lomu gēnu aktivizēšanā. Viņi pētīja, ar kurām molekulām MECP2 saistās šajā vietā, papildus DNS, un atklāja, ka MECP2 tieši mijiedarbojas ar proteīnu kompleksu, ko sauc par RNS polimerāzi II (RNA Pol II). RNA Pol II ir galvenā šūnu iekārta, kas pārraksta DNS RNS. RNS Pol II nevar atrast gēnus viens pats, tāpēc tam ir nepieciešami daudzi kofaktori jeb sadarbojoši proteīni, lai palīdzētu tai veikt savu darbu.
Pētnieki izvirza hipotēzi, ka MECP2 kalpo kā viens no šādiem kofaktoriem, palīdzot RNS Pol II uzsākt transkripciju gēnos, kur saistās MECP2. MECP2 strukturālā analīze ir identificējusi molekulas daļas, kas saistās ar RNS Pol II, un citi eksperimenti ir apstiprinājuši, ka MECP2 zudums samazina RNS Pol II klātbūtni attiecīgajās transkripcijas sākuma vietās, kā arī mērķa gēnu ekspresijas līmeņus.
Tas liek domāt, ka Reta sindromu var izraisīt MECP2 mērķa gēnu transkripcijas samazināšanās MECP2 mutāciju dēļ, kas neļauj tam saistīties ar RNS Pol II vai saistīties ar DNS. Saskaņā ar šo ideju visizplatītākās MECP2 mutācijas, kas saistītas ar slimību, ir saīsinājumi: mutācijas, kurās trūkst proteīna daļas, kas var mainīt mijiedarbību starp MECP2 un RNS Pol II.
Pētnieki cer, ka viņu atklājumi ne tikai mainīs mūsu izpratni par MECP2, bet arī, ka dziļāka un plašāka izpratne par to, kā MECP2 ietekmē smadzeņu attīstību un darbību, var radīt jaunas atziņas, kas palīdzēs cilvēkiem ar Reta sindromu un saistītiem traucējumiem, tostarp autisms.
"Šis projekts ir lielisks Jaenisch laboratorijas darba sadarbības piemērs," saka Flamjē. "Rūdolfam un Yi bija īpaša problēma ar Reta sindromu, un man bija pieredze ar CUT&Tag tehnoloģiju, kas varētu atrisināt šo problēmu. Diskusiju laikā mēs sapratām, ka varam apvienot savus centienus, un tagad mums ir lieliska informācijas krātuve par MECP2 un tās saistību ar slimību."
