Jaunas publikācijas
Iedzimtas imunitātes aktivizēšana: svarīga identificētā mehānisma daļa
Pēdējā pārskatīšana: 14.06.2024

Visi iLive saturs ir medicīniski pārskatīts vai pārbaudīts, lai nodrošinātu pēc iespējas lielāku faktisko precizitāti.
Mums ir stingras iegādes vadlīnijas un tikai saikne ar cienījamiem mediju portāliem, akadēmiskām pētniecības iestādēm un, ja vien iespējams, medicīniski salīdzinošiem pārskatiem. Ņemiet vērā, ka iekavās ([1], [2] uc) esošie numuri ir klikšķi uz šīm studijām.
Ja uzskatāt, ka kāds no mūsu saturiem ir neprecīzs, novecojis vai citādi apšaubāms, lūdzu, atlasiet to un nospiediet Ctrl + Enter.
LMU pētnieki ir atšifrējuši dažādu enzīmu sarežģīto mijiedarbību ap iedzimto imūnreceptoru Toll-like receptor 7 (TLR7), kam ir svarīga loma mūsu ķermeņa aizsardzībā pret vīrusiem.
Toll-like receptor 7 (TLR7), kas atrodas uz mūsu imūnsistēmas dendritiskajām šūnām, spēlē izšķirošu lomu mūsu dabiskajā aizsardzībā pret vīrusiem. TLR7 atpazīst vienpavedienu vīrusu un citas svešas RNS un aktivizē iekaisuma mediatoru izdalīšanos. Šī receptora disfunkcijai ir arī galvenā loma autoimūno slimību gadījumā, padarot TLR7 aktivācijas mehānisma izpratni un, ideālā gadījumā, modulēšanu vēl svarīgāku.
Pētnieki, kurus vadīja profesors Veits Hornungs un Marlina Berouti no Minhenes Ģenētikas centra un LMU Bioķīmijas katedras, varēja iedziļināties sarežģītajā aktivizācijas mehānismā. Iepriekšējos pētījumos bija zināms, ka sarežģītas RNS molekulas ir jāsagriež, lai receptors tās atpazītu.
Izmantojot dažādas tehnoloģijas, sākot no šūnu bioloģijas līdz krioelektronu mikroskopijai, LMU pētnieki ir atklājuši, kā tiek apstrādāta vienpavediena svešā RNS, lai noteiktu TLR7. Viņu darbi tika publicēti žurnālā Imunity.
Svešas RNS atpazīšanā ir iesaistīti daudzi fermenti
Evolūcijas laikā imūnsistēma specializējās patogēnu atpazīšanā pēc to ģenētiskā materiāla. Piemēram, iedzimto imūnreceptoru TLR7 stimulē vīrusa RNS. Mēs varam domāt par vīrusu RNS kā par garām molekulu virknēm, kas ir pārāk lielas, lai tās atpazītu par TLR7 ligandiem. Šeit palīgā nāk nukleāzes — molekulārie griezējinstrumenti, kas sagriež “RNS virkni” mazos gabaliņos.
Endonukleāzes sagriež RNS molekulas pa vidu kā šķēres, bet eksonukleāzes sagriež pavedienu no viena gala līdz otram. Šis process rada dažādus RNS gabalus, kas tagad var saistīties ar divām dažādām TLR7 receptoru kabatām. Tikai tad, kad abas receptoru saistošās kabatas ir aizņemtas ar šiem RNS gabaliem, tiek aktivizēta signalizācijas kaskāde, kas aktivizē šūnu un izraisa trauksmes stāvokli.
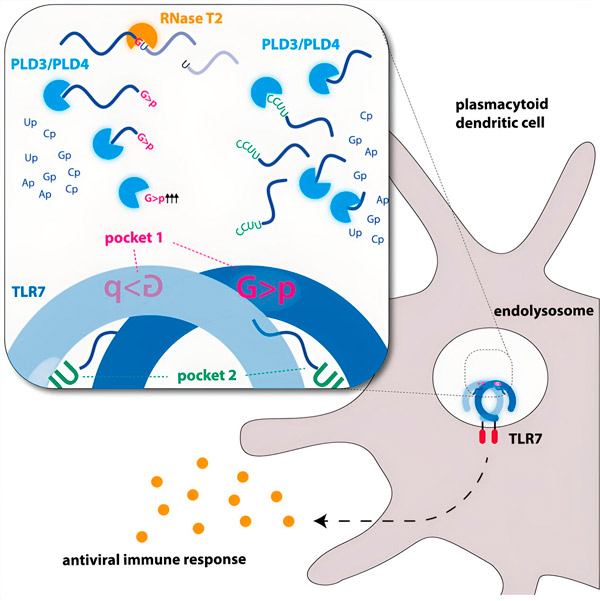
Grafisks attēls. Avots: Immunity (2024). DOI: 10.1016/j.immuni.2024.04.010
Pētnieki ir atklājuši, ka TLR7 RNS atpazīšanai nepieciešama endonukleāzes RNāzes T2 aktivitāte, kas darbojas kopā ar eksonukleāzēm PLD3 un PLD4 (fosfolipāze D3 un D4). "Lai gan bija zināms, ka šie fermenti var noārdīt RNS," saka Hornungs, "tagad esam pierādījuši, ka tie mijiedarbojas un tādējādi aktivizē TLR7."
Imūnsistēmas līdzsvarošana
Pētnieki arī atklāja, ka PLD eksonukleāzēm imūnās šūnās ir divējāda loma. TLR7 gadījumā tiem ir pretiekaisuma iedarbība, savukārt citam TLR receptoram TLR9 ir pretiekaisuma iedarbība. "Šī PLD eksonukleāžu dubultā loma liecina par precīzi koordinētu līdzsvaru, lai kontrolētu pareizas imūnās atbildes," skaidro Berouti.
"Šo enzīmu vienlaicīga iekaisuma stimulēšana un kavēšana var kalpot kā svarīgs aizsardzības mehānisms, lai novērstu sistēmas disfunkciju." Kāda loma šajā signalizācijas ceļā var būt citiem fermentiem un vai iesaistītās molekulas ir piemērotas kā terapijas mērķi, tiks pētīta turpmāk.
