Jaunas publikācijas
"Skābeklis šūnām": vienkāršs implants palīdzēja pazemināt cukura līmeni bez spēcīgām zālēm
Pēdējā pārskatīšana: 18.08.2025

Visi iLive saturs ir medicīniski pārskatīts vai pārbaudīts, lai nodrošinātu pēc iespējas lielāku faktisko precizitāti.
Mums ir stingras iegādes vadlīnijas un tikai saikne ar cienījamiem mediju portāliem, akadēmiskām pētniecības iestādēm un, ja vien iespējams, medicīniski salīdzinošiem pārskatiem. Ņemiet vērā, ka iekavās ([1], [2] uc) esošie numuri ir klikšķi uz šīm studijām.
Ja uzskatāt, ka kāds no mūsu saturiem ir neprecīzs, novecojis vai citādi apšaubāms, lūdzu, atlasiet to un nospiediet Ctrl + Enter.
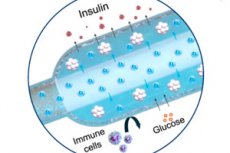
Žurnālā Nature Communications tika aprakstīts jauns “skābekļa” implants 1. tipa diabēta ārstēšanai: kompakts elektroķīmiskais skābekļa ģenerators (iEOG) nepārtraukti piegādā O₂ makrokapsulai ar insulīnu izdalošām šūnām. Šī sistēma ļauj cieši iepakot izolētas saliņas (līdz 60 000 IEQ/ml) un saglabā to dzīvotspēju un sekrēciju pat zema skābekļa apstākļos. Žurkām ar diabētu zem ādas implantētā ierīce uzturēja normālu cukura līmeni līdz pat trim mēnešiem — bez imūnsupresijas. Kontroles grupas žurkām bez skābekļa saglabājās hiperglikēmija.
Fons
- Galvenā tehniskā problēma ir skābeklis. Tiklīdz mēs šūnas “paslēpjam” aiz membrānas un ievietojam ierīci zem ādas (ērti un viegli izvelkama), tām trūkst skābekļa: difūzija caur membrānu un slikti apasiņoto vietu neapmierina “rijīgo” saliņu vajadzības. Līdz ar to notiek agrīna bojāeja, vāja darbība un nepieciešamība ievērojami retināt sēklu – pretējā gadījumā kapsula izrādās milzīga.
- Kāpēc tas ir tik fiziski grūti? Skābeklis caur audiem pārvietojas tikai ļoti īsos attālumos, un iekapsulētām šūnām nav savu asinsvadu – pirmos mēnešus tās dzīvo tikai pasīvas difūzijas dēļ. Jebkura materiālu sabiezēšana vai šūnu "sablīvēšanās" ātri pārnes kapsulas centru uz hipoksiju.
- Ko esi iepriekš mēģinājis?
- Viņi izgatavoja ar skābekli uzpildāmas makroierīces (piemēram, βAir): iekšpusē ir rezervuārs, kas katru dienu tiek papildināts ar skābekli; ir veikti preklīniskie un agrīnie klīniskie pētījumi. Tas darbojas, bet pacientam ir darbietilpīgi.
- Tika izmēģināti ķīmiskie O₂ donori un "nesējmateriāli" (perfluora savienojumi): tie palīdz, bet dod īslaicīgu un grūti kontrolējamu efektu. Parādījās arī "gaisa" rāmji O₂ piegādes paātrināšanai gēla biezumā.
- Pašas kapsulas un implantācijas vietas (plānas membrānas, prevaskularizācija) tika uzlabotas, taču bez ārēja O₂ avota tās joprojām sasniedz šūnu blīvuma robežas.
- Kādu robu mīklā aizpilda jaunais darbs? Žurnāla Nature Communications autori parāda nepārtrauktu skābekļa piegādi no mini ģeneratora tieši makrokapsulācijas sistēmā: ierīce ņem ūdeni no audiem un elektroķīmiski izdala O₂, kas vienmērīgi "elpo" pa kapsulu ar šūnām. Ideja ir piešķirt kapsulai savu "akvārija kompresoru", lai tā varētu iesaiņot vairāk šūnu un joprojām uzturēt tās dzīvas un darbspējīgas – pat zemādas, ne pārāk "skābekļa piesātinātā" vietā.
Kāpēc tas vispār ir nepieciešams?
Saliņu jeb beta šūnu transplantācija ir viens no daudzsološākajiem ceļiem uz 1. tipa diabēta "funkcionālu izārstēšanu". Taču pastāv divi galvenie šķēršļi:
- Imunitāte — parasti nepieciešama mūža imūnsupresantu lietošana;
- Skābekļa bads — kapsulas, kas aizsargā imūnsistēmu, vienlaikus atdala šūnas no asinsvadiem, un beta šūnas, kas rijīgi meklē O₂, ātri "nosmak". Jaunais pētījums sasniedz otro barjeru: tas piešķir kapsulai savu, kontrolētu skābekļa avotu.
Kā darbojas implants
- Divas daļas. Titāna korpusā atrodas mini skābekļa ģenerators (iEOG), kas no intersticiālā šķidruma iegūst ūdeni un elektrolīzes ceļā atbrīvo O₂; blakus tam atrodas plāna lineāra kapsula ar šūnām (līdzīga garai "desai"), caur kuru iet gāzu caurlaidīga caurule: skābeklis vienmērīgi tiek absorbēts pa visu kapsulu. Starp šūnām un audiem ir puscaurlaidīga membrāna (elektrospinējums + algināts): glikoze un insulīns iziet cauri, imūnās šūnas ne.
- Izmēri: iEOG otrās versijas diametrs ir 13 mm, biezums — 3,1 mm, un tā sver aptuveni 2 g. Savienota pārī ar kapsulu, šādu sistēmu var ievietot un izņemt caur nelielu iegriezumu, kas ir svarīgi drošības nolūkos.
- Produktivitāte. Ģenerators saražo ~1,9–2,3 cm³ O₂/h un uztur norādīto plūsmu mēnešiem un pat gadiem ilgi (ilgtermiņa testos fizioloģiskā šķīdumā — līdz 2,5 gadiem), un pēc implantācijas žurkām šis līmenis tika saglabāts. Šāda plūsma ir aprēķināta, lai segtu simtiem tūkstošu saliņu ekvivalentu vajadzības — tādā apjomā, kāds nepieciešams cilvēkam.
Ko parādīja eksperimenti
- In vitro: Pie 1% O₂ (smaga hipoksija), skābekļa pievadīšana uzturēja dzīvotspēju un sekrēciju INS-1 agregātos un cilvēka saliņās, kas bija iepakotas ļoti blīvā slānī (60 000 IEQ/ml).
- In vivo (žurkām). Pēc subkutānas implantācijas alogēnā diabēta modelī iEOG sistēma normalizēja glikēmiju līdz pat 3 mēnešiem bez imūnsupresijas; ierīcēm bez skābekļa nebija nekādas ietekmes. Histoloģijā ap ģeneratoru netika konstatētas būtiskas blakusparādības.
Kāpēc tas ir svarīgi klīnikai?
- Solis pretī “reālistiskiem izmēriem”. Lai pieaugušajam nodrošinātu devu 300–770 tūkstoši IEQ, kapsulai jābūt cieši iepakotai – to vienmēr ir ierobežojis skābeklis. Kontrolēta O₂ padeve “noņem griestus” attiecībā uz blīvumu un dod iespēju padarīt ierīci pietiekami kompaktu reālai implantācijai.
- Plus ērtības. Iepriekš mēs izmēģinājām ķīmiskos skābekļa donorus (peroksīdus) — tie neiedarbojas ilgi un ir nekontrolējami, kā arī O₂ rezervuārus ar ikdienas "uzpildīšanu" caur ādu — apgrūtinošus un neērtus. Šeit skābeklis tiek piegādāts pastāvīgi un izmērītās devās, bez injekcijām.
Tehniskas detaļas, kas iespaido
- Ūdens avots ir audi. iEOG caur porainu “logu” uzsūc intersticiālā šķidruma tvaikus, un pēc tam, izmantojot klasisku membrānas-elektroda mezglu (MEA) un 1,4–1,8 V spriegumu, ūdens tiek atdalīts H₂ un O₂; gāzes tiek aizvadītas pa dažādiem kanāliem.
- Izturība. Trīs ierīces fizioloģiskā šķīdumā darbojās 11 mēnešus, 2 gadus un 2,5 gadus ar līdzstrāvu, un skābekļa plūsma nedeva tām nekādas izmaiņas; pēc implantācijas imūndeficīta un imūnkompetentām žurkām veiktspēja saglabājās.
Ierobežojumi un "kas tālāk"
Tas joprojām ir pirmsklīniskais posms: žurkas, augsts blīvums kapsulā, skābekļa padeve — viss ir lieliski, bet galvenie testi vēl priekšā:
- mērogošana atbilstoši cilvēku devām un laika periodiem;
- elektroķīmiķu uzticamība un barošanas avots cilvēka ķermenī gadiem ilgi (barošanas avota arhitektūra rakstā nav detalizēti aprakstīta);
- fibrozes samazināšana ap kapsulām un difūzijas stabilitāte;
- testēšana ar beta cilmes šūnām un cilvēkiem tuvākos modeļos. Autori atklāti salīdzina savu risinājumu ar iepriekšējām pieejām un pozicionē to kā platformu klīniski translējamām kapsulām.
Secinājums
Lai transplantētās beta šūnas varētu dzīvot un funkcionēt bez imūnsupresantiem, tām ir jāelpo. Kornela un partneru komanda parādīja, ka lineārā kapsulā iebūvēts mini skābekļa ģenerators var pietiekami ilgi un vienmērīgi “pabarot” šūnas ar O₂, lai tās izturētu augstu blīvumu un samazinātu cukura līmeni pat zemādas vietā. Līdz klīnikai vēl ir tāls ceļš ejams, taču inženiertehniskā loģika ir vienkārša un skaista — dot šūnām gaisu tur, kur tā trūkst.
