Jaunas publikācijas
Periodontīta šūnu mehānismu noskaidrošana, izmantojot uzlabotu dzīvnieku modeli
Pēdējā pārskatīšana: 02.07.2025

Visi iLive saturs ir medicīniski pārskatīts vai pārbaudīts, lai nodrošinātu pēc iespējas lielāku faktisko precizitāti.
Mums ir stingras iegādes vadlīnijas un tikai saikne ar cienījamiem mediju portāliem, akadēmiskām pētniecības iestādēm un, ja vien iespējams, medicīniski salīdzinošiem pārskatiem. Ņemiet vērā, ka iekavās ([1], [2] uc) esošie numuri ir klikšķi uz šīm studijām.
Ja uzskatāt, ka kāds no mūsu saturiem ir neprecīzs, novecojis vai citādi apšaubāms, lūdzu, atlasiet to un nospiediet Ctrl + Enter.
Tokijas Medicīnas un zobārstniecības universitātes (TMDU) pētnieki ir izstrādājuši metodi, kas ļauj detalizēti analizēt periodontīta attīstību laika gaitā.
Periodontālā slimība, kas pazīstama kā periodontīts, ir galvenais zobu zaudēšanas cēlonis un skar gandrīz katru piekto pieaugušo visā pasaulē. Vairumā gadījumu šo stāvokli izraisa iekaisuma reakcija uz bakteriālu infekciju audos ap zobiem.
Stāvoklim pasliktinoties, smaganas sāk atkāpties, atsedzot zobu un kaula saknes. Jāatzīmē, ka periodontīta sastopamība palielinās līdz ar vecumu, un, tā kā pasaules iedzīvotāju skaits pieaug, ir svarīgi labi izprast tā pamatcēloņus un progresēšanu.
Pētījumā, kas publicēts žurnālā Nature Communications, TMDU pētnieki atrada veidu, kā sasniegt šo mērķi, uzlabojot plaši izmantotu dzīvnieku modeli periodontīta pētīšanai.
Tieši pētīt periodontītu cilvēkiem ir sarežģīti. Tāpēc zinātnieki preklīniskajos pētījumos bieži izmanto dzīvnieku modeļus. Piemēram, "ligatūru izraisīta periodontīta peles modelis" ir ļāvis pētniekiem pētīt šūnu mehānismus, kas ir šī stāvokļa pamatā, kopš tā ieviešanas 2012. gadā.
Vienkārši sakot, šis modelis mākslīgi izraisa periodontītu, uzliekot zīda diegus uz peļu dzerokļiem, izraisot aplikuma uzkrāšanos. Lai gan šī metode ir ērta un efektīva, tā neatspoguļo visu periodontīta ainu.
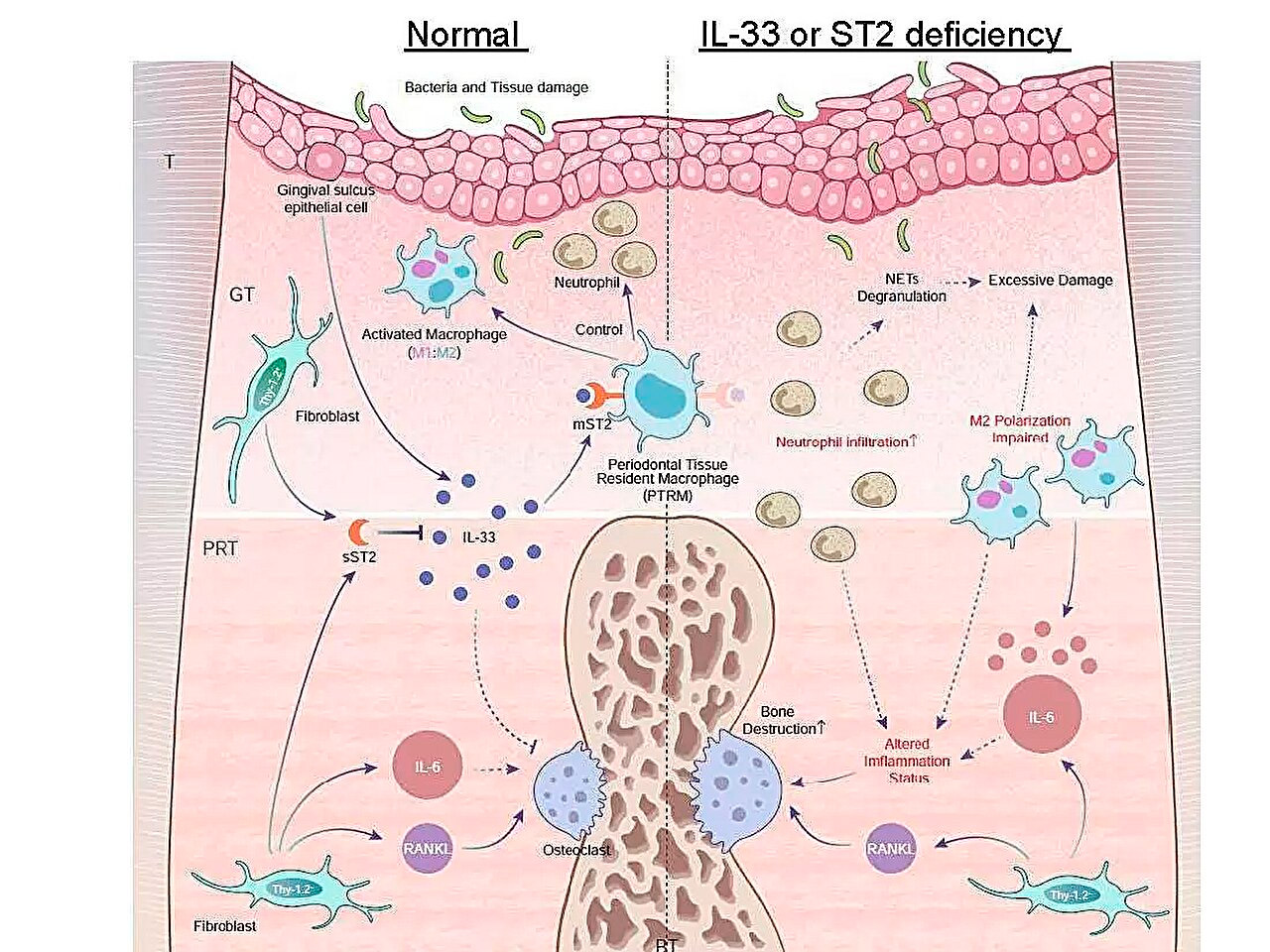
Iekaisuma gēnu ekspresijas profilu shematisks attēlojums periodontīta laikā un IL-33/ST2 ass loma akūta iekaisuma apkarošanā. Avots: Tokijas Medicīnas un zobārstniecības universitāte.
"Lai gan periodonta audi sastāv no smaganām, periodonta saitēm, alveolārā kaula un cementa, analīze parasti tiek veikta tikai ar smaganu paraugiem tehnisku un kvantitatīvu ierobežojumu dēļ," norāda vadošais pētījuma autors Anhao Liu. "Šī paraugu ņemšanas stratēģija ierobežo secinājumus, ko var izdarīt no šiem pētījumiem, tāpēc ir nepieciešamas metodes, kas ļauj vienlaikus analizēt visus audu komponentus."
Lai risinātu šo ierobežojumu, pētnieku komanda izstrādāja modificētu ligatūras izraisīta periodontīta modeli. Klasiskās vienas ligatūras vietā viņi izmantoja trīskāršu ligatūru uz vīriešu dzimuma peļu augšējā kreisā molāra. Šī stratēģija paplašināja kaulaudu zuduma laukumu, būtiski neiznīcinot kaulu ap otro molāru, palielinot dažādu periodonta audu veidu skaitu.
"Mēs izolējām trīs galvenos audu tipus un novērtējām RNS ražu starp abiem modeļiem. Rezultāti parādīja, ka trīskārši ligētais modelis efektīvi palielināja ražu, sasniedzot četras reizes lielāku normālo periradikulāro audu daudzumu un atbalstot dažādu audu tipu augstas izšķirtspējas analīzi," skaidro vecākais autors Dr. Mikihito Hajaši.
Pēc modificētā modeļa efektivitātes apstiprināšanas pētnieki nolēma pētīt periodontīta ietekmi uz gēnu ekspresiju dažādos audu tipos laika gaitā, koncentrējoties uz gēniem, kas saistīti ar iekaisumu un osteoklastu diferenciāciju.
Viens no viņu galvenajiem atklājumiem bija tas, ka Il1rl1 gēna ekspresija bija ievērojami augstāka periradikulārajos audos piecas dienas pēc ligācijas. Šis gēns kodē ST2 proteīnu receptoru un mānekļa izoformās, kas saistās ar citokīnu, ko sauc par IL-33, kurš ir iesaistīts iekaisuma un imunoregulācijas procesos.
Lai iegūtu dziļāku ieskatu šī gēna lomā, komanda izraisīja periodontītu ģenētiski modificētām pelēm, kurām trūka vai nu Il1rl1, vai Il33 gēna. Šīm pelēm tika novērota paātrināta iekaisuma kaulu destrukcija, kas uzsver IL-33/ST2 ceļa aizsargājošo lomu. Turpmāka šūnu, kas satur ST2 proteīnu tā receptoru formā, mST2, analīze atklāja, ka lielākā daļa no tām ir cēlušās no makrofāgiem.
"Makrofāgi parasti tiek iedalīti divos galvenajos veidos: pro-iekaisuma un pretiekaisuma, atkarībā no to aktivācijas. Mēs atklājām, ka mST2 ekspresējošās šūnas bija unikālas ar to, ka tās vienlaikus ekspresēja dažus abu veidu makrofāgu marķierus," komentēja vecākais autors Dr. Takanori Iwata. "Šīs šūnas atradās periradikulārajos audos pirms iekaisuma sākuma, tāpēc mēs tās nosaucām par 'periodonta audu rezidentu makrofāgiem'."
Kopā šī pētījuma rezultāti parāda modificēta dzīvnieku modeļa spēju pētīt periodontītu detalizētākā mērogā, līdz pat biomolekulāram līmenim.
"Mēs piedāvājam iespēju, ka jauns IL-33/ST2 molekulārais ceļš regulē iekaisumu un kaulu destrukciju periodonta slimībā, kā arī specifiski makrofāgi periradikulārajos audos, kas ir dziļi iesaistīti periodonta slimībā. Cerams, ka tas novedīs pie jaunu ārstēšanas stratēģiju un profilakses metožu izstrādes," secina vecākais autors Dr. Tomoki Nakashima.
